С этой главы начинается биохимическая линия учебника, и ее главы будут заметно более углубленными, чем разные генетические и цитологические. Просто потому, что детализация клеточных процессов при переходе на биохимический уровень неизбежно возрастает: если при обсуждениях функций ДНК в клетке мы оперируем крупными объектами типа хромосом и веретена деления, то сейчас мы начнем разбираться в отдельных небольших молекулах и их взаимодействиях. Возможно, тебе захочется читать эту главу несколько дней — например, пробежать ее для начала как художественную и отложить, а потом вернуться и уже вдумчиво изучить какую-то часть, а потом снова отложить. Пусть необходимое для изучения наук углубление происходит постепенно и приносит удовольствие.
Вообще очень удобно начинать влезать в биохимию параллельно изучению цитологии и генетики, потому что так у тебя будет складываться более полная картина происходящего. И ты сможешь переключаться между разными уровнями детализации, настраивая свой «интеллектуальный микроскоп».
По моему опыту во время погружения в какую-то одну науку на несколько дней или недель иногда хочется смены направления: например, отложить страстно всасываемую цитологию и залезть в биохимию. Возникает восприятие, что немного уставший и офигевший от обилия цитологической информации мозг набрасывается на биохимию с новыми силами, как будто и не пахал в две смены всю прошлую неделю. Иногда раз в день хочется делать такие отвлечения на другую науку от основной, и тоже есть эффект «отдохнувшего мозга» при переключении. У меня есть предположение, почему так происходит: во время изучения цитологии активнее всего задействованы нейронные связи, отвечающие за цитологические понятия (типа «клетка», «ткань», «лизосомы»), ведь именно их я больше всего использую, дополняю новой информацией, связываю с новыми словами. А когда я переключаюсь на биохимию, то задействованы другие понятия, а значит включаются другие нейронные связи, которые были отдохнувшими и поэтому активно работают. Конечно же, связь «клетка», которая использовалась и раньше, довольно часто вспыхивает, но тут основная нагрузка будет не на нее: я ведь залезаю глубоко внутрь клеток и разглядываю молекулы, а значит понятие «клетка» используется только как некий общий абрис. Интересно будет когда-нибудь эту теорию проверить, а сейчас пора переходить к содержанию этой главы, запуская «биохимические» нервные цепи (а у тебя они начинают создаваться между прочим!).
Если ты прочитала предыдущие главы генетической линии, то ты в курсе, что такое аденин. И привыкла к тому, что это просто один из кирпичиков, используемых для построения молекул ДНК или РНК. Теперь придется отвыкать:), потому что это далеко не единственное его применение в наших клетках. И на самом деле в ДНК и РНК используется не просто аденин, а его соединение с другими молекулами. Просто до сих пор нам было достаточно такого вот приближения, чтобы не перегружать твой мозг длинными непроизносимыми терминами.
Ну вот теперь стоит в этих самых терминах разобраться, потому что всякие «аденин», «аденозин», «аденозинтрифосфат», которые мы будем использовать по мере погружения в науки все чаще, очень похожи и непонятно в каких отношениях друг с другом находятся. А есть еще более сложные непроизносимые слова типа «дезоксирибонуклеотид», и вроде как они соотносятся с предыдущими, но понять, как именно, уже невозможно, потому что мозг отключился еще на прочитывании «аденозинтрифосфата». Можешь его включить опять, потому что больше такого перегруза терминами не будет, пусть вылезает из раковины. В этой главе мы стараемся использовать минимум терминов и подробно объяснять значение встречающихся, поэтому в итоге вместо смутно знакомого слова «АТФ» у тебя будет ясность о том, из каких частей эта штука состоит, и что с ней можно делать.
Изучая генетику и цитологию вот так, как это делаем мы — сначала рисуя ее общими, крупными мазками, можно попутно углубляться в какие-то мелкие, но очень важные детали. Делать это стоит постепенно, не перегружая свою память, не формируя эффекта неприятной усталости и отторжения, а оставаясь в состоянии приятной усталости и предвкушения узнавать новое, или не уставая вовсе. Если запоминать что-то детально и подробно время от времени, то можно получать сильное удовольствие от того, что в каком-то вопросе тебе удалось разобраться довольно-таки глубоко, и многие вещи, которые раньше понимались в общих чертах, теперь приобретают особую глубину и ясность понимания. Тогда и память будет становиться постепенно все более цепкой, объем знаний будет расти, и со временем ты начнешь схватывать и усваивать информацию, лишь пробежав взглядом по тексту.
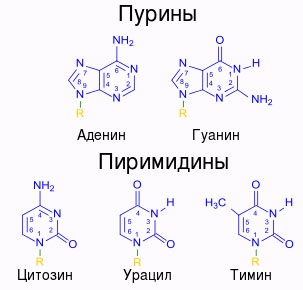
К таким вещам, которые приятно и важно было бы запомнить детально, относится структура главных кирпичиков нашей жизни — азотистых оснований — тех самых, которые входят в состав нуклеотидов, и которые составляют «лесенки» той спирали, которая состоит из двух нитей ДНК, комплементарных друг другу.
Я настоятельно советую начать только с одного азотистого основания! Иначе все начнет путаться, ведь они очень похожи, и вместо удовольствия ты получишь смутное недовольство. И для выбора аденина в качестве первого из них есть особые причины, которые станут ясны позже. Остальные нуклеотиды будет запомнить ОЧЕНЬ легко, если тебе удастся очень хорошо запомнить структуру аденина, и схожешь азотистых оснований уже будет играть нам на руку вместо того, чтобы запутывать. Сначала путем небольшой перестановки молекул мы получим из аденина гуанин, а потом доберемся и до пиримидинов — тимина, урацила и цитозина. Но сначала — аденин и только он.
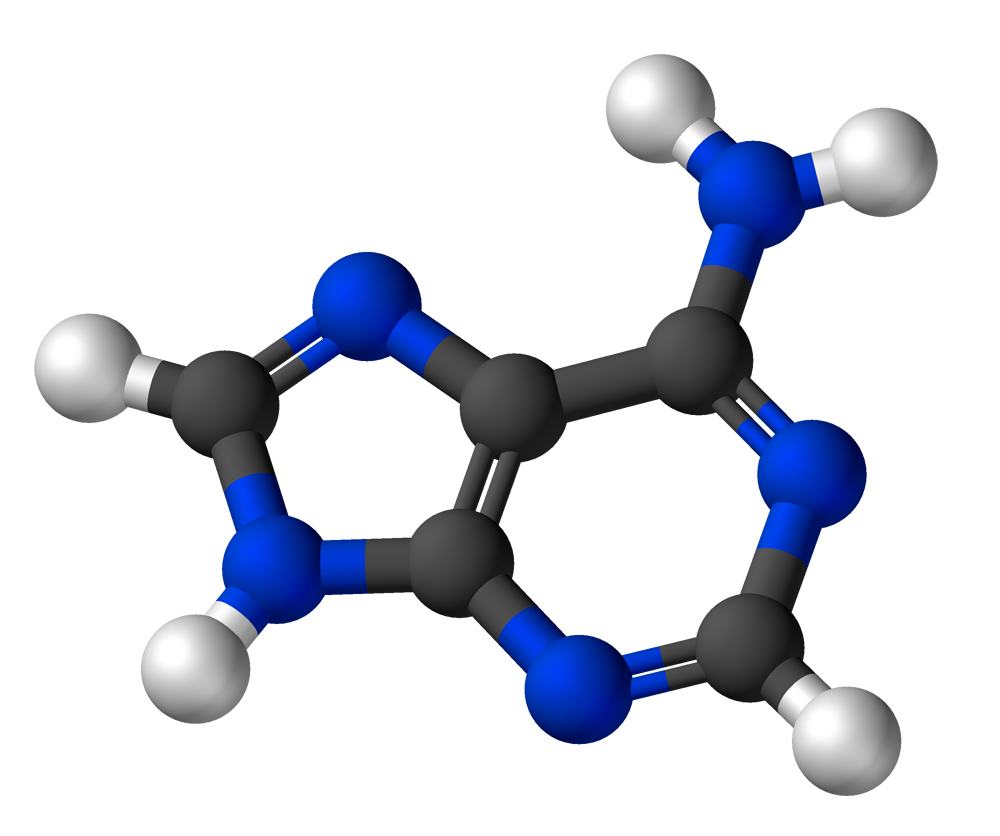
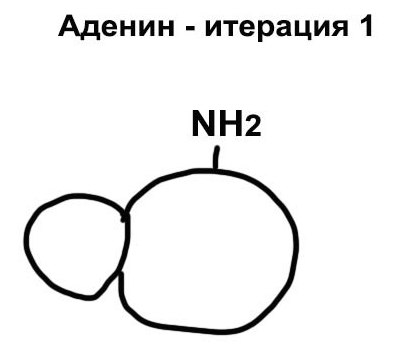
Обратим внимание, что он состоит из двух колец, а значит он относится к классу пуринов. Сверху к большому кольцу приделан хвостик аминогруппы NH2. Научиться отличать пурины от пиримидинов очень просто: у пуринов название короткое, зато сами они крупнее, чем состоящие из одного кольца пиримидины с длинным названием. Можно взять листок бумаги, положить его перед собой и нарисовать самую грубую схему аденина: мелкое кольцо, справа к нему боком примыкает кольцо покрупнее, и сверху большого кольца — NH2. То, что я нарисовала, ты видишь справа: это итерация номер 1. Не так уж плохо, кстати, получилось:). Даже такое представление об аденине — уже очень неплохо. И на этом можно пока что остановиться, пойти позавтракать или поиграть с собакой. Спустя минут пять спроси себя — помнишь ли ты эту схему? Можешь ее легко нарисовать? И если да, то почему бы не начать читать эту главу дальше?
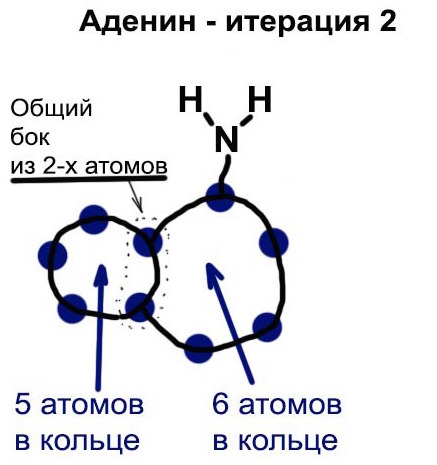
Давай теперь подсчитаем — сколько атомов в меньшем, и сколько в большем кольце? Пять и шесть. Отлично. Нарисуем эти пять и шесть атомов и обратим внимание, что оба кольца имеют общий бок, состоящий из двух атомов. А аминогруппу группу NH2 нарисуем тоже в виде реальных атомов, как они и расположены в молекуле — в виде такой рогатки. Теперь у нас есть итерация номер 2, и это уже довольно круто! Съешь яблоко, позвони другу, а спустя несколько минут спроси себя — можешь ли ты нарисовать схему-2? И если нет, то в этом нет вообще ничего странного или страшного. Наша память постепенно приспосабливается к запоминанию новых видов информации, и она приспособится — важно начать. А у тебя всегда есть полно других интересов (надеюсь), на которые можно отвлечься, время от времени проверяя — точно ли тебе теперь запомнилась схема 2.
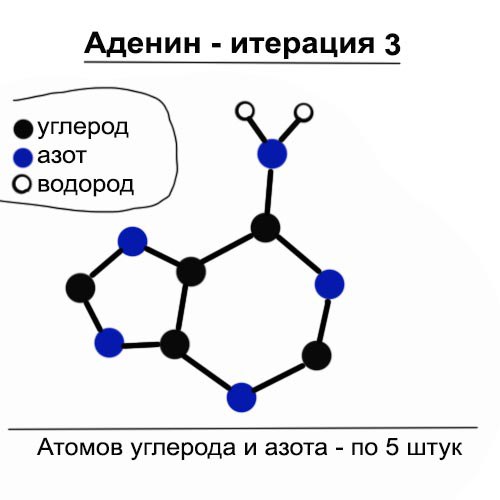
Дальше давай разберемся с атомами углерода. В конце концов, они — главные элементы органических молекул. На основном рисунке внизу они обозначены черными шариками и на них написана белая буква «С». Мы сделаем точно то же самое и на своем новом рисунке (справа). И тут легко запомнить, что все те атомы в структуре колец, которые НЕ являются углеродом, являются азотом. Давай углерод обозначим на рисунке черными кружками, а азот — синими. Два атома водорода в аминогруппе обозначим колечками. Легко заметить, что атомов азота и углерода в аденине — по пять штук. Это можно использовать для проверки своих картинок.
Вот. Мы получили уже очень точную картину аденина. Для того, чтобы запомнить схему 3, тебе может быть придется совсем отвлечься на другие дела, в течение дня время от времени посматривать на схему, и возможно только завтра или даже послезавтра ты сможешь уверенно ее рисовать. И это отлично. Главное — запомнить прочно, с удовольствием.
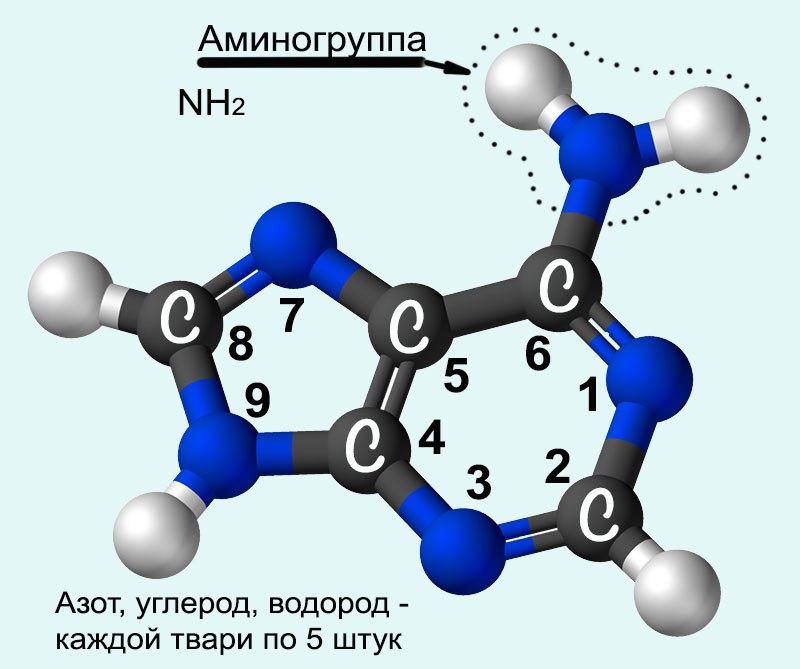
И на самом деле, этого уровня для наших целей вполне достаточно. Ты можешь обратить внимание, что на последней — самой полной красивой схеме — атомы в кольцах пронумерованы. Это довольно удобно для некоторых целей, но в общем на данном этапе это запоминать необязательно. Хочется — запомни, это пригодится. Не хочется — и не надо, потом как-нибудь.
Еще ты можешь увидеть, что между некоторыми атомами имеется одинарная связь, то есть у них есть одна общая пара электронов, а между другими атомами — двойная связь, и значит у них две общих пары электронов — именно этими обобществленными парами электронов атомы и образуют химические связи. Об этом у нас будет подробно в других главах. И мы видим, что атомов водорода тоже пять штук. Удобно. Если тебе хочется — постепенно запомни места размещения двойных связей и атомов водорода, не хочется — запомнишь потом, тем более, что есть определенная закономерность, связывающая количество межатомных связей и количество атомов водорода, приклепленных к другим атомам, и когда ты узнаешь эту закономерность ( я говорю о валентности — для тех, кто в курсе), то запомнить итоговую схему станет намного проще.
Так что уже сейчас ты знаешь как выглядит аденин — пусть даже на уровне итерации 1. Спустя пару дней в твоей голове прочно закрепится итерация 3, и этого ВПОЛНЕ достаточно для наших целей. Более подробно запомнить совсем не обязательно — только если именно захочется потренировать память.
Итак, аденин — это молекула, состоящая из двух колец, имеющих общие два атома и несколько торчащих в стороны атомов. Сама по себе, отдельно эта молекула клеткой не используется, а вот в соединении с другими молекулами аденин становится незаменимой штукой, которая участвует в самых разных процессах.
Аденин называют азотистым основанием (потому что кроме обычного для органики углерода в них содержится азот), и в клетке есть похожие на него молекулы — другие азотистые основания. Мы про них тут уже упоминали: это еще один пурин (гуанин) и три пиримидина (тимин, цитозин и урацил). С некоторыми из них ты знакома все по тем же главам про ДНК и РНК, потому что эти две молекулы строятся из нуклеотидов, где главной частью является как раз азотистое основание. Сейчас пытаться их запомнить тем более не нужно, мы занимаемся аденином! Выплюнь гуанин из головы, потом возьмешь. А просто для впечатлений и чтобы их похожесть ты увидела не только на словах, я добавляю сюда их схемы.
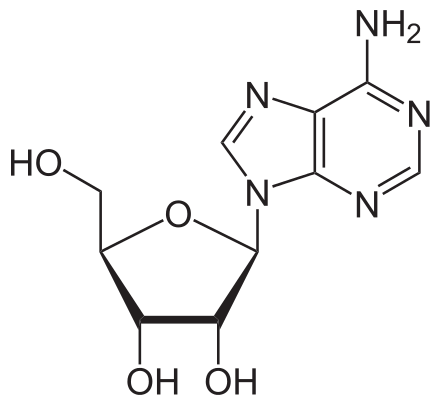
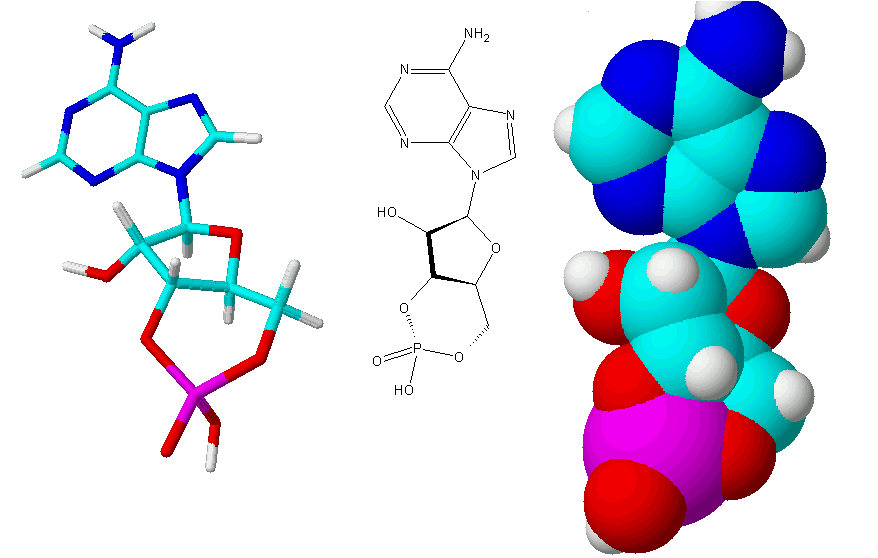
Но до нуклеотидов мы еще дойдем в этой главе, а пока посмотри на промежуточный этап между азотистым основанием и нуклеотидом: аденозин. Такие промежуточные штуки называют нуклеозидами, и в их состав могут входить любые азотистые основания. В верхнем правом углу схемы аденозина ты видишь тот самый двухкольцевой аденин. Только к одному из атомов азота меньшего кольца приделали еще одно пятиугольное «кольцо на ножках и с хвостом». Вот с этого кольца на ножках, которое представляет собой молекулу сахара, и начинается первая путаница у непосвященных, но хотящих приобщиться к биохимии (это я про собственный опыт). Потому что в нуклеозидах могут содержаться ДВА разных вида сахаров, отличающихся всего лишь ОДНИМ атомом. Казалось бы, в молекуле из почти тридцати атомов одним атомом больше, одним меньше — какая разница? А она есть:), и подробно про нее ты можешь прочитать в главе про РНК.
Чтобы в этой главе не было путаницы, и чтобы подготовить почву для следующей биохимической главы, здесь будут нуклеозиды и нуклеотиды только с одним из сахаров: рибозой. Ее молекула и присоединена к аденину на схеме вверху, а с другим сахаром разберемся позже. Аденозин — в отличие от аденина — уже имеет отдельную роль в организме, а не только входит в состав активных молекул. Некоторые нейроны обмениваются сигналами с его помощью, и предполагают, что эти нейроны отвечают за стимуляцию сна и подавление бодрости.
Кофеин может вмешиваться в этот процесс, присоединяясь к нейронным рецепторам вместо аденозина и блокируя их. Из-за этого выпущенный в качестве сигнального вещества аденозин не может соединиться с рецептором, натыкаясь на кофеиновую «заглушку», и нейроны не могут передать сигнал о том, что организм устал и ему неплохо бы поспать. При этом человек ощущает бодрость, которая не является отражением состояния его тела, а вызвана воздействием кофеина — в общем, результат не очень привлекательный. Несмотря на это «кофеин» не равен «кофе», польза которого уже доказана, в том числе и для предотвращения возникновения рака, так что не стоит быть фанатиком и запрещать себе его пить. Ну и к тому же не только в кофе содержится кофеин, несмотря на название — например, в «общеизвестно полезном» зеленом чае он тоже есть. В умеренных дозах типа одного американо в первой половине дня негативных последствий от содержащего кофеин напитка не должно быть даже у тех, чей организм дольше обычного расщепляет эти молекулы. Да, оказывается, что у разных людей процесс разбирания кофеина на части протекает по-разному, и зависит это от их ДНК.
В XXI веке, вооружившись информацией о своем геноме, ты можешь получить генетически обоснованные рекомендации по питанию. И зная, какой вариант гена CYP1A2 ты унаследовала, решить: с кофеином или без будет твоя следующая чашка капучино. Потому что именно от гена CYP1A2 зависит, с какой скоростью в твоем организме разлагается кофеин. И если ответ на этот вопрос — «медленное расщепление», то последствия от выпитой чашки кофе с кофеином могут оказаться и посущественнее, чем просто бессонная ночь. Ученые полагают, что в этом случае вполне вероятно повышение давления крови.
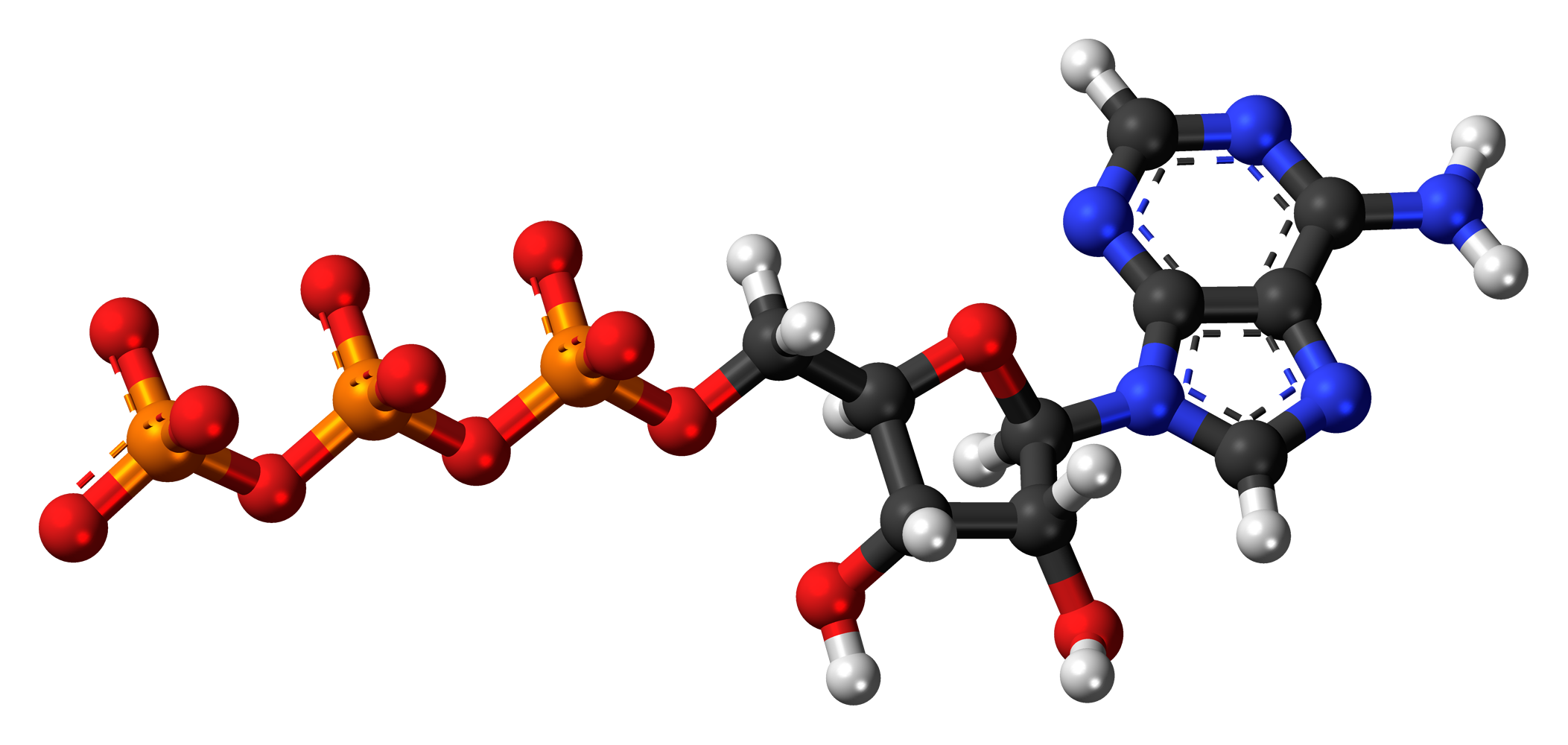
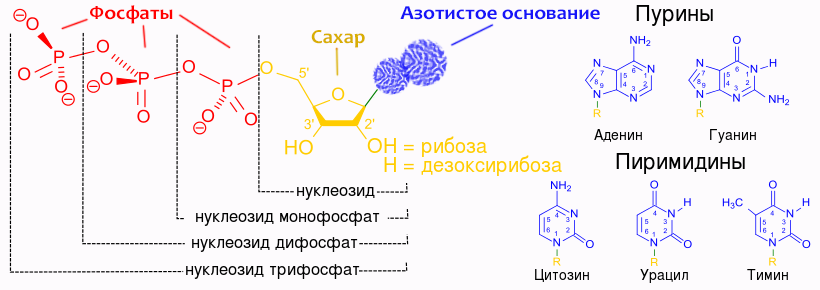
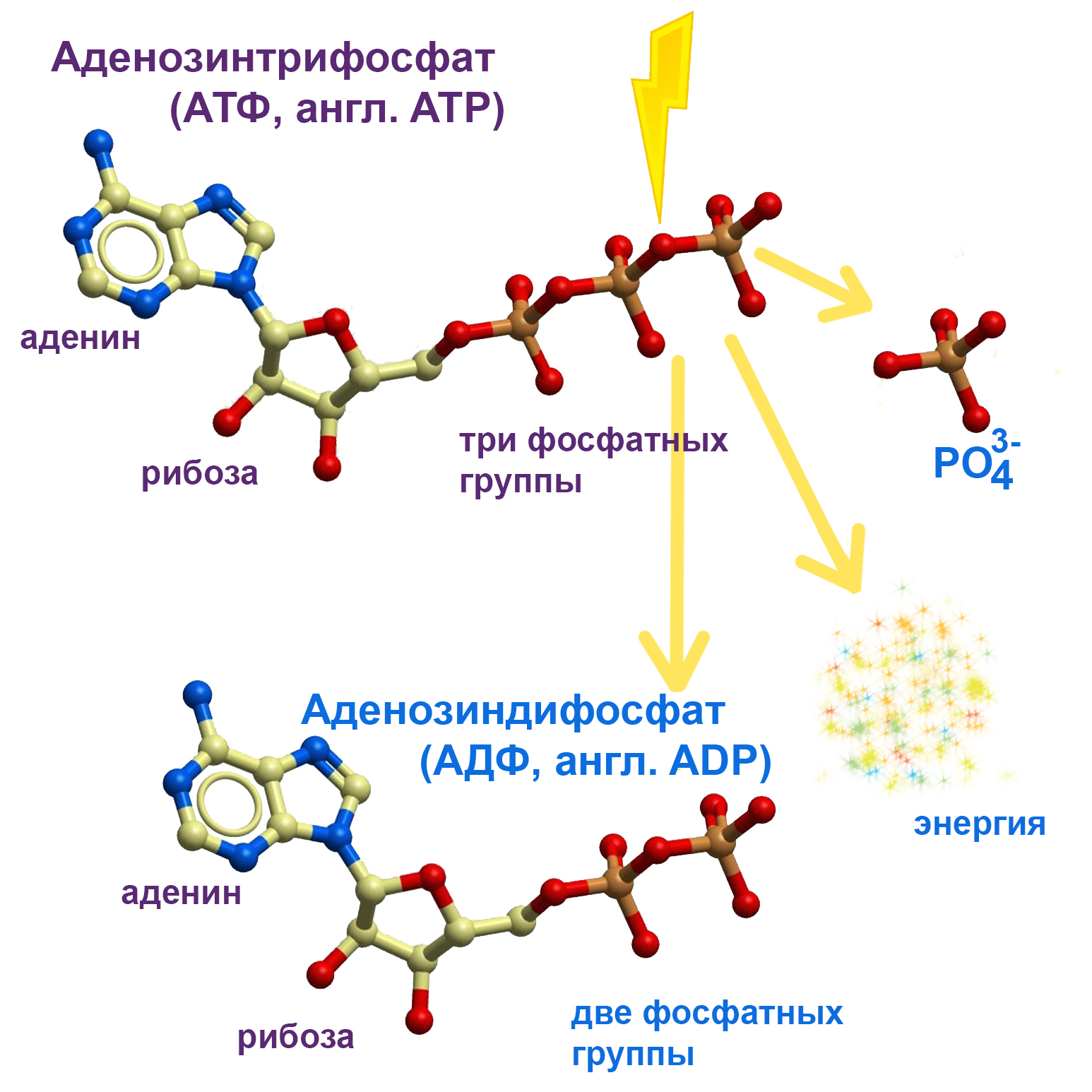
Если ты вместе с чашкой какого-нибудь латте уже всосала информацию об аденине и нуклеозидах, то можно смело переходить к нуклеотидам. Это самая простая часть, потому что нуклеотиды получают из нуклеозидов, добавляя одну и ту же молекулу к любому из них. Эта молекула — фосфат. На схеме слева ты видишь уже знакомые черно-синий аденин и черно-красную рибозу, а длинный красно-оранжевый хвост — это как раз три последовательно соединенных фосфата. Вообще в этом хвосте может быть другое количество фосфатов — два или один. И в любом варианте вся молекула будет называться нуклеотидом.
С одной стороны, это кажется не очень удобным — что одно и то же слово может обозначать немного отличающиеся молекулы. А с другой стороны, часто для понимания написанного нам и не нужно знать, сколько у какого-то нуклеотида фосфатов. Когда такая информация является существенной, пользуются полными и точными названиями этих молекул. Например, если взяли основавние аденин, присоединили к нему сахар рибозу и добавили один фосфат, получился аденозинМОНОфосфат. «Аденин + рибоза» = «аденозин», а к нему добавлен одинокий МОНО-фосфат. Оказывается, это длинное название вполне выговариваемое, если понимать, что оно означает. Записывать это удобно как АМФ, так что жизнь становится еще проще. Если к аденозину добавили два фосфата, то «моно» заменяется на «ди», и записывают название получившегося нуклеотида как АДФ. И так далее.
Если важно указать, какой в нуклеотиде используется сахар, то про ту молекулу, схема которой висит выше говорят, что это рибонуклеотид. Именно рибонуклеотиды используются для построения молекул РНК — рибонуклеиновой кислоты. С ДНК на самом деле тоже все просто: в ней используется другой сахар, в котором не хватает одного атома кислорода. А без этого атома кислорода это уже не рибоза, а ДЕЗОКСИрибоза. «Дез-» означает «без», «-окси-» от английского «oxygen» — кислород. Так что «дезоксирибонуклеотид» — это всего лишь название нуклеотида, в состав которого входит дезоксирибоза. Опять же — не пытайся все это запомнить: достаточно иметь смутное представление обо всех этих молекулах и связях между ними, чтобы в следующий раз тебе было проще про них читать из-за возникающего узнавания. Если опять рассмотреть процесс изучения чего-то нового с точки зрения нейронных цепей в мозге, то ты сейчас «протаптываешь дорожки» новых связей между нейронами. Пока они совсем слабые, потому что только что появились, но чем больше ты ими будешь пользоваться (например, читая другие главы «Живомордности», статьи Википедии на смежные темы, научно-популярные книжки по генетике и т.п.), тем прочнее они будут становиться, и тем легче информация будет усваиваться.
Вот в этой таблице подведен итог всех разбирательств с названиями похожих молекул. Если раньше при виде ее кому-нибудь из читателей могло стать не очень хорошо, то сейчас ты наверняка имеешь примерное понимание того, что означают все эти обозначения. Этого понимания вполне достаточно, чтобы читать главу дальше. Всякие подробности о том, как устроены нуклеотиды, постепенно запомнятся просто от чтения глав об их использовании клеткой.
Рибонуклеотид АденозинТриФосфат, или АТФ ( Adenosine triphosphate, ATP ) наверное самый известный среди всех нуклеотидов — из-за того, что он выполняет больше всего функций в клетке. Поэтому в этой главе и уделяется наибольшее внимание аденину, а остальные азотистые основания ждут своей очереди на получение места жительства в твоем мозге. Причем функции АТФ сильно отличаются друг от друга, и возникает вопрос: почему одна и та же молекула используется так по-разному? Предполагают, что это произошло потому, что клетки развивались постепенно: сначала они имели немного функций, пользовались для их выполнения какими-то молекулами, и периодически учились чему-то новому, если оказывалось что с этой новой функцией жизнь становилась комфортнее. И когда они это новое действие осваивали, они брали для его выполнения то, что лежало «под рукой»: какие молекулы имелись внутри клетки в изобилии, те и использовались. Если у тебя есть приятель-геймер, у которого в квартире скопилась куча деталей от древних компьютеров, то ты же не очень удивишься, что в качестве горшка для своей коллекции кактусов он использует системный блок? Вот и клетки не заморачивались на тему — а будет ли логично молекулу, которую мы используем как строительный блок, использовать еще и для запасания энергии, и для передачи сигналов? Попалась, пригодилась, удобно — заточили инструменты под эту молекулу и пользуемся. А вслед за этими клетками-прародителями и все мы делаем то же самое, потому что настолько древние механизмы изменять нельзя: одно малейшее изменение — и вся тщательно отлаженная система с пригнанными друг к другу деталями зашатается и рухнет.
Так вот всех видов рибонуклеотидов в древних клетках было навалом, потому что из них строятся РНК. Были там и гуаниновые, и цитозиновые, и урациловые — почему же самым популярным, то есть наиболее используемым, стал именно АТФ? Может быть, это результат простой случайности: именно та клетка, которая активно его использовала, оставила больше потомков, а они еще больше потомков, и так далее, пока не дошло до нас. Или именно пуриновое азотистое основание дает больше возможностей для его использования, удобнее в применении, чем пиримидиновое. В пользу последнего говорит тот факт, что гуанозинтрифосфат, или ГТФ, используется в клетках для тех же целей, что и АТФ, просто не в таком объеме, поэтому мы и начали описание с «главного» из этих двух нуклеотидов. А азотистое основание ГТФ (гуанин) тоже является пурином.
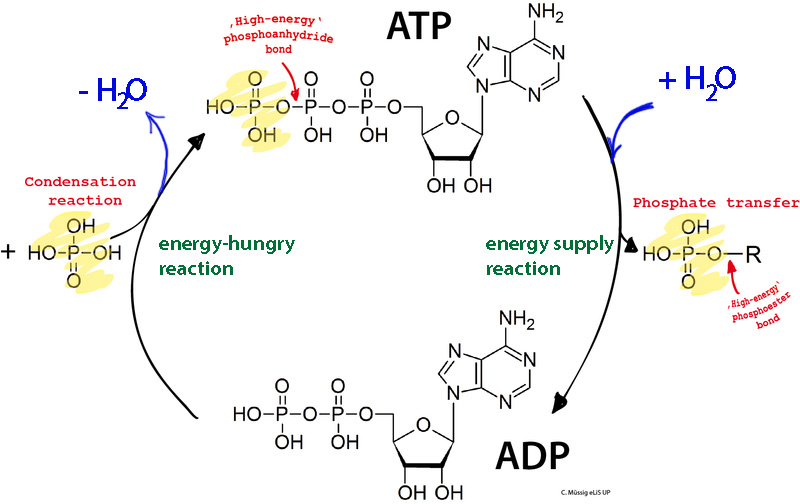
При всех использованиях клеткой АТФ ее аденозиновая часть остается нетронутой. Клеточные ферменты покушаются только на фосфатный хвост: они то откусывают эти фосфаты (обычно по одному), то наоборот берут молекулы АМФ или АДФ и достраивают их до АТФ. Потому что если фосфат откусывается, это приводит к выделению большого количества энергии, и клетка ее пускает на какие-то свои нужды. А если у клетки есть энергия, которую ей нужно запасти, то она начинает «чеканить валюту», то есть создавать молекулы АТФ. Сами по себе, без влияния ферментов они не разрушаются. А значит, потраченная на их создание энергия надежно хранится в виде целого трехфосфатного хвоста. И в любой момент она может быть использована. Можешь рассмотреть схему внизу, чтобы эта информация уложилась. На ней изображен круговой цикл: создание молекулы АТФ с затратами энергии и добавлением фосфата к молекуле АДФ, и обратный процесс — отщепление фосфата от АТФ с выделением энергии и образованием АДФ. Ежесекундно в каждой твоей клетке происходят бесчисленные количества таких циклов.
Уже сейчас ты довольно глубоко погрузилась в биохимию, потому что заметь — речь идет о манипуляциях с группами атомов, запасании энергии в связях между этими группами. Возможно, сейчас стоит сделать очередной перерыв, отложить главу на несколько часов, а потом рассмотреть эту схему — понятно ли, что это за молекулы и что с ними происходит? Если в общих чертах понятно, то можно двигаться дальше. Если нет, то ты же никуда не торопишься? Пролистай еще раз главу до этого места, и в зависимости от настроения или отложи ее, или двигайся дальше.
А дальше хочется разобраться — зачем вообще все эти откусывания и присоединения фосфатов к аденозину, что они дают?
1. Можно взять молекулу АТФ и использовать ее при создании РНК в качестве одного из «кирпичиков». Из множества таких кирпичиков-нуклеотидов получится в итоге очень полезная для клетки молекула: она будет или чертежом для построения протеина, или служебной молекулой, выполняющей одну из сотен функций в клеточном метаболизме.
Добавить в состав РНК можно не любой нуклеотид, а только тот, у которого есть три фосфата. Потому что во время встраивания от нуклеотида откусывают сразу два фосфата: выделяющаяся при этом энергия используется, чтобы присоединить нуклеотид к строящейся молекуле РНК. Оба фосфата при этом уплывают от места стройки и болтаются в цитоплазме, пока их как-нибудь не используют. Например, для создания новой молекулы АТФ. А оставшийся при нуклеотиде фосфат является важной частью РНК, одним из кирпичиков ее «хребта», из которого торчат азотистые основания. На стилизованном изображении РНК справа этот «хребет» изображен в виде толстой золотистой трубы, из которой торчат палочки — азотистые основания. Это как раз самое привычное нам использование АТФ, и поэтому хватит про него, двигаемся дальше.
2. АТФ используется самыми разными ферментами, чтобы добывать энергию на их ферментативные нужды. Про ферменты мы немного писали тут, а в общем можно просто сказать что это такие штуки, которые умеют из двух небольших молекул создавать одну большую. Или наоборот, брать одну молекулу и ее разбирать на части. И на то, и на другое требуется энергия, и ферменты часто используют ту, которая была запасена в виде молекулы АТФ. Уже понятно, что и в этом случае от АТФ будут откусываться фосфаты, но в отличие от построения РНК обкусанные ферментом АДФ или АМФ не встраиваются в какую-нибудь молекулу. Иногда они просто выпускаются назад в клетку, а иногда остаются присоединенными к ферменту — до того момента, пока их не заменит полная фосфатов молекула АТФ, и цикл не запустится заново. Если тебе стало интересно, как вообще может энергия запасаться в молекуле, про это есть отдельная глава учебника.
Итак: был АТФ, фермент от него откусил фосфатную группу и использовал выделившуюся энергию, а куда делась фосфатная группа? Тут тоже могут быть варианты:
* она выпускается в клетку и плавает отдельно — так же, как в случае использования АТФ для построения нуклеотида
* она присоединяется к тому протеину, который обрабатывался ферментом, расщепившим АТФ. Такой протеин с присоединенным фосфатом называют фосфорилированным. Это присоединение маленькой группы атомов (в фосфате всего лишь один атом фосфора и четыре кислорода) имеет совсем не маленькие последствия, и когда ты узнаешь в чем они заключаются, твой взгляд на живую материю будет уже несколько иным.
Во-первых, фосфат имеет отрицательный заряд. Ну это на самом деле ничем необычным не является — соединились атомы фосфора и кислорода, и электрический заряд на такой молекуле никого не удивит. Противоречит нашим интуиции и «бытовому здравому смыслу» то, что НА ПРОТЕИНАХ тоже есть и положительные, и отрицательные заряды! Можно ли представить что-то менее похожее на магнит, чем кусок белка? И вообще кажется, что электричество касается неорганических веществ — всяких железок, компьютеров и роботов. Ну стекло и пластмасса конечно могут намагничиваться, и твои волосы тоже, но все равно большая часть электричества, с которой мы сталкиваемся, связана с металлами. А тут вдруг откуда-то появились положительные и отрицательные электрические заряды на белках.
На самом деле твоя интуиция не ошибается. Если взять обычный белок из вареного яйца, он конечно же не будет притягиваться к магниту. А вот если настроить наш воображаемый микроскоп на большее увеличение и рассмотреть какую-нибудь молекулу, поместив ее в магнитное поле, то тебя может ждать сюрприз. Потому что есть молекулы, которые несут на себе заметный электрический заряд: например, ДНК заряжена отрицательно! То есть поднеси к ней магнит, и она на него отреагирует — подплывет ближе или отодвинется подальше. На этом ее свойстве основаны разные методы исследования ДНК: молекулы разной длины помещают в гель (чтобы они двигались медленнее, чем в жидкости), пропускают электрический ток через получившееся «желе с начинкой из ДНК» и смотрят, как под воздействием тока молекулы ДНК двигаются. Самые длинные из них будут сильнее застревать в геле и двигаться медленно, а самые короткие подберутся ближе всех к тому месту, где находится положительный заряд.
Но если то же самое проделать с хромосомой (состоящей, как ты знаешь, из ДНК и протеинов, на которые эта ДНК намотана), то такого поразительного эффекта не будет. Потому что протеины, входящие в состав хромосом, заряжены положительно — это как раз помогает им удерживать намотанную нить ДНК. И если рассматривать хромосому как единое целое и на это целое воздействовать электрическим током, она останется в величавой неподвижности: положительные заряды протеинов компенсировали отрицательные заряды ДНК, и эта большая штука оказывается электрически нейтральной. Но если ты будешь рассматривать ее на большем уровне приближения, когда станут видны отдельные атомы, то тут уже невозможно не заметить присутствие небольших, но вездесущих электрических зарядов.
Итак, молекулы твоего тела, в том числе протеиновые, имеют положительные и отрицательные заряды на своих частях. И эти заряженные части взаимодействуют друг с другом не хуже магнитных шариков из модной игрушки: разноименные заряды притягиваются друг к другу, одноименные отталкиваются. И под воздействием этих сил молекулы приобретают свою форму и свои функции. Протеины в результате этого не болтаются в клетке длинной сосиской из соединенных друг с другом аминокислот, а сворачиваются, приобретая ту самую форму, которая позволяет им выполнять их функции.
Теперь вернемся к фосфорилированию — добавлению к такой вот покрытой электрическими зарядами молекуле отрицательно заряженного фосфата. Если развивать аналогию с магнитными шариками, то это все равно что к лежащим на поверхности и образующим какую-то фигуру шарикам добавить еще один: остальные шарики, оказавшиеся в поле досягаемости электрического заряда новичка, как-то на него отреагируют, изменят свое положение. Их изменение положения в свою очередь изменит их влияние на соседей, а значит и те будут двигаться — получится такая расходящаяся от нового добавленного шарика волна изменений. В протеинах происходит то же самое: добавленный отрицательно заряженный фосфат взаимодействует с другими заряженными частями протеина, и они сдвигаются под воздействием электромагнитного взаимодействия, образуя новую конфигурацию (то есть способ сворачивания). И в результате возможны два варианта развития событий:
1. Если протеин до этого был не активным, то есть был свернут так, что не мог выполнять какую-нибудь функцию, то из-за присоединения фосфата он сворачивается иначе. И это дает ему возможность выполнять ранее недоступную функцию.
2. Если протеин был активным без присоединения фосфата, то фосфорилирование его «выключит» — тоже за счет изменения его формы.
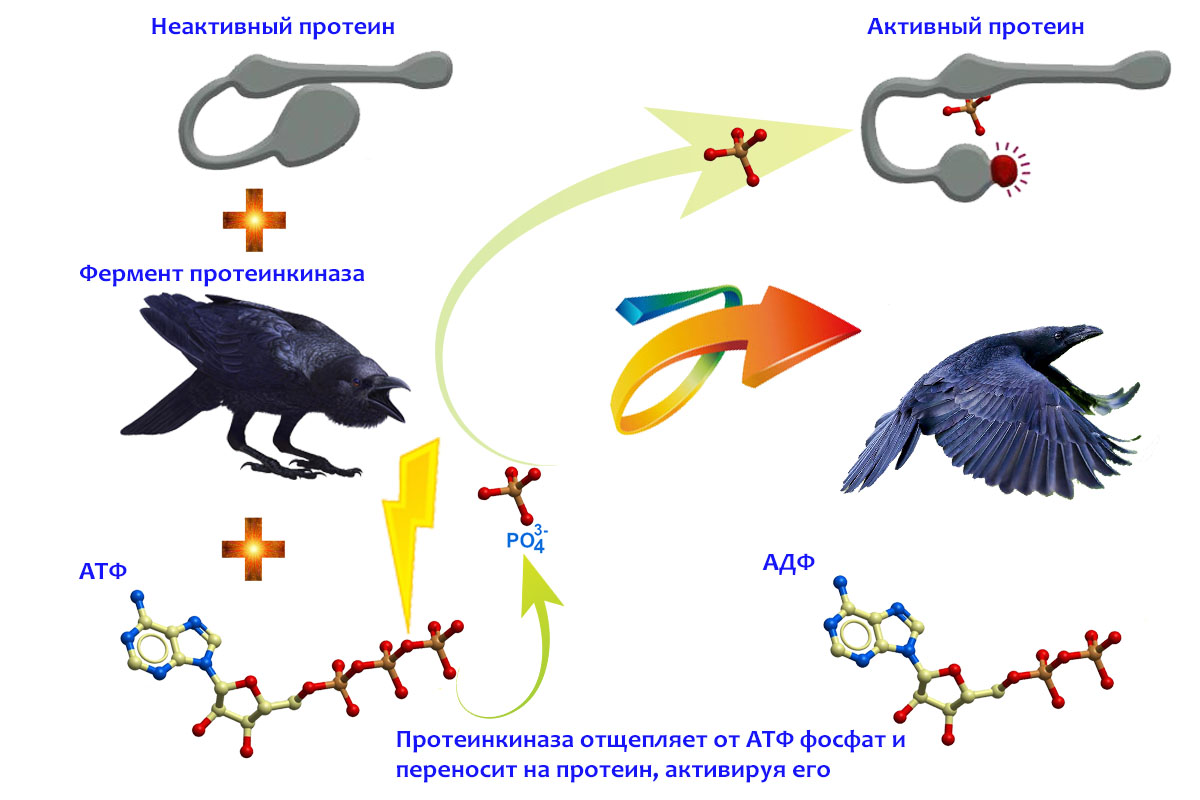
Ферменты, предназначение которых — откусывание фосфата от АТФ и присоединение его к протеину, называются протеинкиназами. Это большой класс ферментов, и выглядят разные его представители по-разному, и выбирать какой-то один из них для общей схемы активности протеинкиназ нет смысла. Поэтому роль протеинкиназ на схеме фосфорилирования выполняют вороны:
Пока ты рассматриваешь эту картинку, информация о том, как происходит фосфорилирование, аккуратно укладывается у тебя в голове. Тут ты видишь вот что:
? сначала у протеина была одна форма, и он был не активным. А потом на него налепили фосфат, и форма изменилась — просто потому, что этот фосфат встал как распорка между его двумя частями. Та часть протеина, которая до сих пор была плотно прижата, освободилась, и именно она будет выполнять какую-то протеиновую функцию.
? протеинкиназа переносит фосфат от молекулы АТФ на протеин, после чего она теряет интерес к обеим этим молекулам и улетает.. ну то есть уплывает, чтобы фосфорилировать следующий попавшийся протеин. Молекула АТФ, лишившаяся фосфата, превратилась в АДФ и тоже уплывает.
3. Третий способ использования АТФ клеткой очень сильно отличается от предыдущих двух. В первом способе АТФ был кирпичиком для построения РНК, и в то же время источником энергии для собственного присоединения к создающейся молекуле. Во втором способе АТФ прежде всего источник энергии, но помимо этого он иногда выступает «донором» фосфата для манипуляций с протеином.
Для того, чтобы использовать АТФ третьим способом, от нее откусывают две фосфатных группы, а оставшийся фосфат крепче присоединяют к рибозе (той пятиугольной штуке, которая торчит посередине нуклеотидов). Такие молекулы называются циклическим аденозинМонофосфатом, или просто цАМФ ( Cyclic adenosine monophosphate, cAMP ).
цАМФ являются сигнальными молекулами: они расплываются в разные стороны от того места в клетке, где их сделали, попадают на протеинкиназы (помнишь этот фермент из предыдущего пункта, который прилепляет фосфаты на протеины?), прикрепляются к ним и таким образом активируют. Пока цАМФ не присоединился к протеинкиназе, она будет плавать не активированная, и никакие протеины, которые она может обрабатывать, не будут фосфорилированы. И только когда клетка получила сигнал, означающий что пора эти протеинкиназы запустить в действие, она производит цАМФ и они передают этот сигнал дальше, к протеинкиназам.
Такой способ передачи сигнала позволяет его многократно усиливать: достаточно активировать одну молекулу, занимающуюся переработкой АТФ в цАМФ, и она начинает штамповать их без перерыва, пока ее не выключат. То есть одна активная молекула создаст много молекул-передатчиков сигнала. А каждая уплывшая цАМФ может активировать одну протеинкиназу, которая, став активной, займется своим любимым делом — будет навешивать фосфат на один протеин за другим. Это уже второй этап усиления сигнала, а началось ведь все с одной активной молекулы!
Передачи сигналов между клетками и внутри них — одна из самых интересных и запутанных тем биохимии. Потому что в каждой клетке таких сигнальных путей несколько, и они могут друг с другом пересекаться, влиять один на другой, усиливать друг друга или наоборот подавлять. Сейчас известно несколько таких путей и идет активное их изучение — прежде всего для того, чтобы разобраться в механизмах работы клетки и научиться в них вмешиваться для достижения каких-нибудь полезных для людей целей. Например, для того, чтобы лечить болезни, связанные с нарушениями в таких сигнальных путях.
Подробное и простое описание одного из них — в следующей главе биохимической линии, где главную роль играет все тот же АТФ.