Наиболее известная и изученная часть иммунной системы состоит из различных специальных клеток (лейкоцитов: фагоцитов, Т-киллеров и прочих зверей, которых иногда упоминали в других главах учебников), выискивающих в организме опасные клетки и вирусы и уничтожающих их. Такими опасными могут быть как чужеродные клетки (например, бактерии, вызывающие какое-либо заболевание), так и собственные клетки организма, по какой-то причине переставшие выполнять свои функции, а то и начавшие приносить вред. Но существует и другая часть иммунной системы, которая представляет собой встроенные в каждую клетку способы сопротивляться инфекции.
Каждая клетка имеет и собственные механизмы противостояния возникшим в ней мутациям, и, кроме этого, еще и способы подачи сигналов клеткам иммунной системы о том, что в ней произошли нарушения. У млекопитающих и птиц помимо этого клетки способны посылать молекулы-оповещения о вторжении вируса. Получив такой сигнал, соседние клетки организма успевают подготовиться к отражению атаки тех самых вирусов, которые уже строятся в зараженной клетке. Передающие это оповещение вещества называются интерферонами ( interferon [ɪntə’fɪərɒn]).
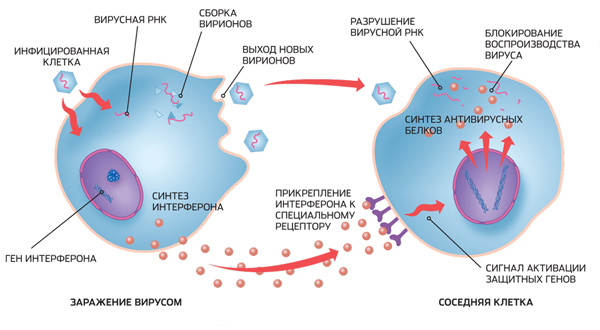
Когда клетка млекопитающего или птицы заражена вирусом, одновременно с производством вирусов она строит протеиновые молекулы (интерфероны), которые проходят через клеточную мембрану и попадают на мембраны соседних клеток. Хотя интерферон не обладает прямым противовирусным действием, то есть например не способен разрушить вирусную наследственную информацию, он способен вызывать такие изменения в клетках, которые препятствуют размножению вируса, формированию вирусных частиц и дальнейшему его распространению.
Важное преимущество интерферонов по сравнению с антителами (молекулами, специфически связывающимися с частями чужеродных бактерий и вирусов, попавших в организм) — их универсальность: они подавляют размножение любого вируса. Конечный результат действия интерферонов представляет собой барьер из устойчивых к вирусу клеток организма, окружающих зараженную клетку, производящую вирусы. Со всех сторон к нему собираются клетки иммунной системы, способные уничтожить зараженную клетку.
Интерферон действует в нескольких направлениях.
Во-первых, попав в клетки, расположенные рядом с инфицированной, он запускает в них цепь событий, приводящих к подавлению синтеза вирусных протеинов, а в некоторых случаях он препятствует еще и сборке и выходу вирусных частиц. Происходит это так:
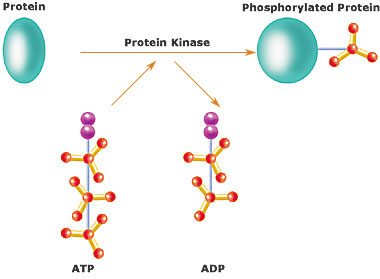
1. Как только в клетку попадают молекулы интерферона, она начинает производство в больших количествах одного из ферментов — протеинкиназы R. Вообще протеинкиназы разных видов выполняют в клетке функции включения или выключения уже находящихся в ней протеинов. Их работа важна для мгновенного реагирования на изменения, происходящие во внешней среде и внутри клетки. Если бы для реакции на опасность или присутствие большого количества пищи нужно было бы создавать новые протеины с нуля, клетка реагировала бы гораздо медленнее, ведь нужно было бы: построить матричную РНК для создания протеинов; построить по этой мРНК протеины; обработать их, доставить в нужные места… Гораздо проще не объявлять и проводить мобилизацию каждый раз с нуля, а заранее иметь «регулярную армию» — какое-то количество протеинов, необходимых для реагирования на стрессовую ситуацию, просто в неактивном виде. И в момент возникновения опасности достаточно будет их включить.
Точно так же с выключением функционирующего протеина: если в какой-то стрессовый момент его активность не полезна клетке, не стоит его тут же разбирать на части, ведь есть основания полагать, что стресс закончится, клеточные процессы должны будут перестроиться на дострессовые, и тогда придется собирать заново большое количество необходимых для спокойной жизни молекул. Поэтому те протеинкиназы, которые отключают протеины, просто навешивают на протеин специальную группу атомов, делающую его неактивным, неспособным выполнять ту функцию, для которой он предназначен. Именно такое выключение и обеспечивает протеинкиназа R, производство которой запускает клетка в ответ на попадание в нее интерферонов.
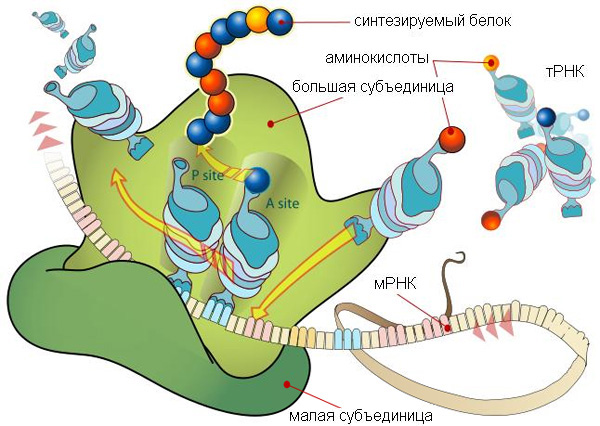
2. Понятно, что протеинкиназа R выключает не все подряд протеины, а только те, которые могли бы использоваться вторгшимся в клетку вирусом для построения новых вирусных частиц. Она нацелена на выключение фактора инициации трансляции: молекулы, без которой рибосома не может начать создавать протеин по матричной РНК. Таким образом синтез протеинов в клетке снижается, но не до нуля, ведь требуется время для деактивации всех молекул инициации трансляции, и какие-то процессы трансляции уже были начаты в момент, когда запустился механизм ее блокировки. Поэтому следующим после производства протеинкиназ R шагом является:
3. производство рибонуклеазы L, которая разрезает все находящиеся в клетке РНК. Особенность рибонуклеазы L в том, что она производится только в ответ на попадание в клетку интерферонов. Она уничтожает все РНК без разбора: и необходимые клетке РНК (матричные и прочие служебные РНК-молекулы). И клеточные РНК-содержащие органеллы, которые могли бы синтезировать вирусные протеины. И вирусные РНК, несущие его наследственную информацию. И создаваемые им матричные РНК для трансляции вирусных протеинов… в общем, такой агент 007 с лицензией на убийство. Понятно, почему производство рибонуклеазы L запускается после выключения факторов инициации трансляции: в то время как это выключение является легко обратимым процессом, рибонуклеаза наносит существенные повреждения, которые могут привести (и часто приводят) к разрушению самой клетки. И запускать этот процесс стоит только в той ситуации, когда попадание интерферонов в клетку носит не кратковременный, а довольно длительный характер, что является признаком того, что соседняя клетка уже давно имеет в себе вирус, до сих пор не уничтожила его и не была уничтожена сама, а значит в любой момент может начать эти вирусы производить, так что стоит встретить их во всеоружии.
Таким образом, когда произведенные зараженной клеткой вирусы выходят из нее и попадают в соседние клетки, они наталкиваются на организованное сопротивление: начать производство протеинов сложно, на вирусную РНК накидываются рибонуклеазы, а клеточные органеллы, которые необходимы для размножения, повреждены. Конечно же, эти повреждения могут привести и к гибели зараженной клетки: если она не сможет быстро справиться с попавшим в нее вирусом, то повреждения станут необратимыми и клетка разрушится вместе с недособранными ею вирусными частицами, что гораздо лучше для организма в целом, чем выживание инфицированной клетки и производство в ней все новых и новых вирусов.
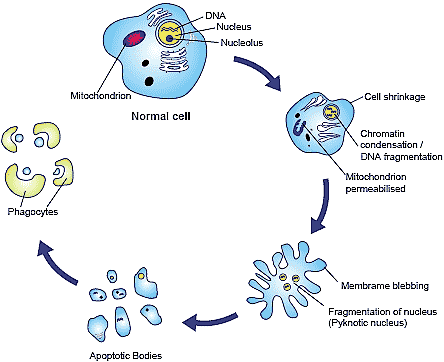
Поэтому вторым направлением действия интерферонов является запуск апоптоза, или запрограммированной гибели клетки.
Апоптоз отличается от других видов разрушения клетки тем, что содержимое клетки (начиная от ДНК и заканчивая органеллами) аккуратно разрезается на подходящие для дальнейшего использования кусочки, которые поглощаются организмом и используются им как источник энергии и строительного материала.
Происходит это так:
1. Попавший в клетку интерферон активирует находящиеся в латентном (то есть неактивном) состоянии протеины p53. В каждой клетке постоянно присутствуют такие протеины, и пока клетка функционирует нормально, они деактивированы. Но как только ДНК клетки существенно повреждается, или если поступает сигнал о возможной атаке вируса, эти протеины становятся активными и выполняют то действие, ради которого клетка постоянно имеет их запас: они связываются с ДНК в определенном месте и запускают считывание гена, продукты которого в большой концентрации и запускают апоптоз.
То, что р53 постоянно присутствует в клетке, и в нужный момент его можно мгновенно активировать, обеспечивает быстрое реагирование клетки на необходимость саморазрушения. А то, что сам р53 не является разрушительным фактором, а всего лишь запускает производство инструментов, начинающих процесс апоптоза, предохраняет клетку от запуска апоптоза по ошибке. Только в случае продолжительного поступления интерферонов уровень р53 будет сохраняться достаточно высоким для того, чтобы клетка саморазрушилась.
2. В процессе апоптоза клеточная ДНК и органеллы нарезаются на кусочки, и клетка распадается на апоптотические тельца: небольшие окруженные мембраной пузырьки жидкости с молекулами, на которые было разрезано клеточное содержимое. Клетка при распаде выделяет в окружающую среду сигнальные молекулы, привлекающие фагоциты (клетки иммунной системы, поглощающие и переваривающие чужеродные тела и разрушающиеся собственные клетки организма).
3. На поверхности мембран апоптотических телец находятся особые молекулы, которые подают фагоцитам сигнал «ешь меня». Фагоциты поглощают их, переваривают (то есть разрезают на удобные для усвоения организмом части) и возвращают в организм для дальнейшего использования. Соседние с распавшейся клетки тоже могут всосать в себя ее части, сразу же пуская в круговорот своих жизненных процессов их содержимое. В среднем от момента запуска апоптоза до поглощения распавшейся клетки проходит 90 минут.
Кроме перечисленных выше первых двух действий (препятствование синтезу вирусных протеинов и запуск апоптоза), интерфероны запускают в клетке процессы активного взаимодействия с клетками иммунной системы. Каждая клетка организма имеет на своей наружной мембране специальные участки, на которых, как на информационном табло, выставляются образцы молекул, соответствующих попавшим в клетку микроорганизмам. Так вот попавший в клетку интерферон приводит к тому, что в ней:
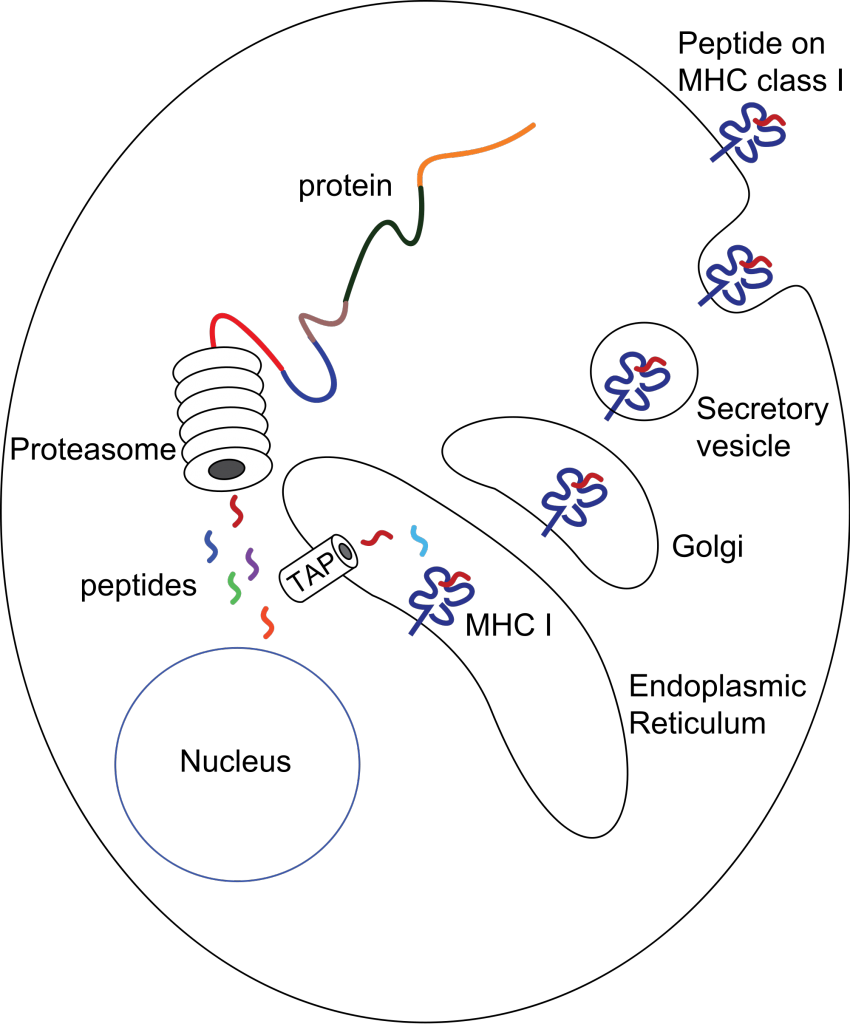
1. Вырабатывается больше строительного материала для этих самых «информационных табло», которые называются главным комплексом гистосовместимости (major histocompatibility complex или MHC).
2. Активируются иммунопротеосомы. От обычных протеосом (органелл, расщепляющих ненужные или поврежденные протеины) они отличаются специализацией на нарезании вирусных компонентов на особенно удобные молекулы для выставления на главном комплексе гистосовместимости.
3. После попадания вируса в активированную таким образом клетку, иммунопротеосомы набрасываются и на впрыснутые вирусом протеины, и на те протеины, производство которых вирус запускает, несмотря на всё оказываемое ему противодействие в клетке. Нарезанные иммунопротеосомами вирусные протеины выставляются на МНС.
4. Существует два вида главных комплексов гистосовместимости. Первый из них (MHC-I) взаимодействует с Т-киллерами и макрофагами — лимфоцитами, специализирующимися на поглощении собственных клеток организма, зараженных вирусами и бактериями, или просто мутировавших до состояния опухолевых.
Когда Т-киллер или макрофаг ползет по клеткам, ощупывая их и проверяя на вкус содержимое их МНС, он останавливается на клетках с сигналом «съешь меня» и приступает к трапезе. Помимо этого, Т-киллер производит гамма-интерфероны. Специфика этого вида интерферонов в том, что кроме уже перечисленных в этой главе функций они изменяют мембраны соседних клеток так, что они становятся менее проницаемыми для вирусов, а также привлекают естественных киллеров (Natural killer cells, или NK cells). NK-киллеры не нуждаются в присутствии главного комплекса гистосовместимости 1 типа на мембране зараженной клетки, и их роль заключается в уничтожении тех зараженных или мутировавших клеток, в которых мутация или клеточный паразит препятствуют образованию MHC-I, делая их неуязвимыми для Т-киллеров. Например, папилломавирус и ВИЧ не дают клеткам-носителям построить MHC-I, поэтому для борьбы с ними гамма-интерфероны необходимы.
5. Второй комплекс гистосовместимости (МНС-II) проверяют Т-хелперы — клетки, активирующие другие лейкоциты. Т-хелперы презентуют другим клеткам иммунной системы фрагменты чужеродных антигенов при прямом контакте, а также привлекают их, выделяя сигнальные молекулы (цитокины). Поэтому выставление вирусных протеинов на MNC-II приводит к резкому усилению иммунного ответа.
Короткий ролик с общей информацией об интерферонах:
Удивительно, что каждая клетка нашего организма способна вырабатывать комплекс веществ, запускающих настолько разнообразные реакции, блокирующие попадающие в него вирусы, не давая им размножаться. Стоит помнить, что эта система не дана нам раз и навсегда в неизменном виде, она непрерывно подстраивается под условия окружающей среды, которые мы сами создаем. Например, если человек усиленно оберегает себя от попадания бактерий и вирусов, его иммунная система «простаивает», и результатом этого могут быть как ее нетренированность и беспомощность перед вторгшимися в итоге болезнетворными агентами, так и неспособность вовремя уничтожать возникающие в организме раковые клетки. Кроме того, за неимением реальных врагов клетки иммунной системы могут атаковать здоровые клетки организма, запуская различные аутоиммунные заболевания.
Одна из идей для тренировки иммунной системы представлена ниже и доступна в основном фут-фетишисткам: